当前位置:首页 >
经典新解:血糖稳态为何成为2型糖尿病制胜关键?
血糖稳态:葡萄糖流入又流出,始终处于动态平衡
为什么一个人不吃饭还能撑这么久?为什么正常人一顿饭不吃虽然会饿,但是不会发生低血糖休克或者死亡?这是因为人体内环境是相对稳定的,内环境稳态是保持正常生命活动和健康的先决条件,主要包括体温、酸碱度、渗透压以及血糖等。
正常生理状态时,葡萄糖流入又流出,人体血糖水平始终处于动态平衡,稳定在3.9~5.6mmol/L(70~100mg/dL),这种状态称之为血糖稳态。血糖稳态本质上是人体维持葡萄糖在生理范围内的一种机制,对于确保大脑、红细胞等依赖葡萄糖供能的细胞发挥正常生理功能具有重要意义。
“131”:血糖稳态维持与调节的核心密码
血糖稳态的维持依赖于机体自主调节系统,涉及到多个器官、组织和激素等精密协作。
第一信使:葡萄糖——“我“调控,”我“自己
葡萄糖是调控人体血糖稳态的“重要信号”,葡萄糖作为血糖调节的第一信使在血糖稳态系统中既是调节变量,也是受控变量。当进餐后,人体能够感知葡萄糖浓度的变化,从而开启核心调糖器官(胰岛、肝脏和肠道)的“自主调节“,从而维持机体的血糖平衡,也就是血糖稳态。
三大核心器官:胰腺、肝脏、肠道
世界著名生理学家坎农强调:稳态不是静态的;相反,它是一个动态的自我调节系统,涉及到各个系统、器官的协调工作,能够在面对不断变化的环境需求时保持生存能力。
血糖稳态的维持依赖于血糖稳态自主调节系统,包括多个参与葡萄糖调控的器官和组织(包括大脑、胰岛、肝脏、肠道、肌肉与脂肪等),它们可感知葡萄糖浓度的变化,分泌血糖调节激素,共同实现血糖稳态调节。其中,胰腺、肝脏、肠道被称为血糖调控核心器官,可根据各自的葡萄糖信号敏锐响应、适时起始升糖或降糖作用。
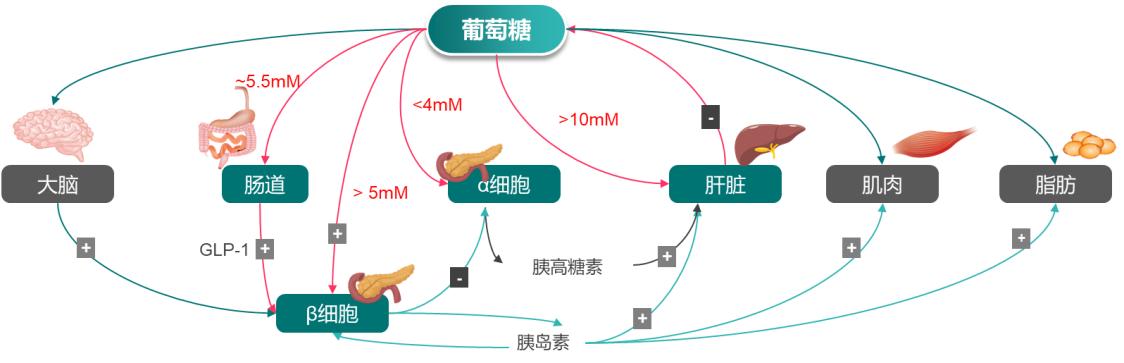
第一关键酶:葡萄糖激酶(GK)
GK同时存在各核心调糖靶器官(肝脏、胰腺及肠道),是血糖调控核心器官细胞内葡萄糖代谢第一个关键酶,当GK敏锐感知到葡萄糖浓度到达葡萄糖调定点后,将葡萄糖信号转换为各器官响应,开启后续的自主调节机制。
在葡萄糖摄取之后,胰岛β细胞感应到血糖浓度高于5 mmol·L-1后,GK被激活,启动胰岛素分泌,同时肠道也因血糖升高而分泌GLP-1,并通过激活在β细胞上的受体,刺激胰岛素的释放;肝脏的GK在血糖升至10 mmol·L-1 后被激活,启动肝糖原合成;当血糖降低到4 mmol·L-1 以下时,GK活性迅速下降,启动胰岛α细胞的胰高血糖素释放机制,胰高血糖素作用于肝细胞的受体,启动肝糖原分解和糖异生机制,机体输送葡萄糖,维持血糖平衡。
2型糖尿病:从修复GK掌握重塑血糖稳态的密码
2021版《 国际糖尿病联盟(IDF)全球糖尿病地图(第10版)》最新数据显示,在过去的10年间(2011年~2021年),我国糖尿病患者人数由9千万增加至1亿4千万,增幅已达56%。虽然在过去三十年间,我国接受治疗的糖尿病患者血糖达标率有所提升(仍不足50%),但IDF最新数据的发布再次提醒我们革命尚未成功的紧迫性!
新药频出,理念变变更,20世纪至今,糖尿病领域经历了“降糖→强化降糖→降糖目标个体化→综合考量患者特征→以患者为中心”的治疗理念变化,用药方案更是尝试殆尽,但为何达标现状仍不足一半?为什么一直无法真正实现糖尿病进展的“逆袭”?
回归疾病发生发展的基本原则,我们是否可以寻得解决问题的端倪?
疾病发生时,稳态被打破,机体降通过复杂的机制进行调节,以建立疾病状态下的新稳态。2型糖尿病建立的新稳态如何?研究显示,血糖失稳态T2DM复杂机制的共同特征,临床表现为“四维指标”不达标,即持续高血糖、餐后血糖、血糖变异性、低血糖的不达标。基础实验和临床试验的进一步探索发现,GK功能降低或许正是导致T2DM血糖失稳态的“罪魁祸首”。
总而言之,血糖稳态维系着我们的代谢健康,在当下的研究当中也取得长足的进步!对于2型糖尿病,修复GK,重塑稳态自主调节正在为广大医生和患者带来新的希望!希望不久的将来,以GK为靶点的血糖稳态治疗方法,能让更多糖尿病患者实现真正的“逆袭”,得到疾病进展的长期缓解!
