当前位置:首页 >
葡萄糖激酶(GK):重塑血糖稳态自主调节核“芯”
“芯片”可通过感知、传递、供能、思考与记忆等功能帮助AI将人类的思考过程信息化、机械化,是当今电子产品及系统更新迭代的核心科技。但归根结底,AI只是试图通过算法去复刻人体的部分功能,人体才是最智能、最精密的系统,这一精密系统的复杂性远远超过现代科技所能窥探的程度,其中最有代表性的当属“血糖稳态系统”。
什么是血糖稳态?简单来说,就是血液中的葡萄糖流入又流出,始终处于动态平衡,从数据上看,正常生理状态时,人体血糖水平稳定在3.9~5.6mmol/L(70~100mg/dL),而这种状态的维持便依赖于血糖稳态自主调节系统。
人们是如何感受血糖水平、并维持血糖稳态的?血糖稳态自主调节系统究竟如何运作?2020年内分泌学界大奖Rolf Luft Award的获得者——宾夕法尼亚大学的Franz Matschinsky教授,为了解开这一疑惑上下求索近半个世纪,如今答案逐渐明了。既往可知,血糖稳态系统涉及多个器官、组织与激素等的精密协作,Franz Matschinsky教授的研究证实,葡萄糖激酶(Glucokinase, GK)集感知、传递功能于一体,可敏锐地感受葡萄糖浓度的变化,启动血糖调控核心器官(胰腺、肝脏、肠道)的升糖/降糖机制,适时调节胰岛素、胰高糖素、GLP-1等控糖激素的分泌,以及肝糖元的合成或分解,介导葡萄糖的存储与利用,从而维持血糖稳态,可谓是真正的调糖之“芯”。
葡萄糖激酶(GK)是什么?
葡萄糖激酶(GK)对于学习过生物化学的人而言,可以说是“最熟悉的陌生人”,因为它是己糖激酶(HK)家族的一种亚型,而HK是细胞内葡萄糖摄取和利用过程中不可或缺的关键酶,是维持促进葡萄糖进入细胞所需的梯度浓度的重要因素。不同HK亚型其功能及其调控存在很大差异,GK独特的分子结构和酶动力学特征,使其成为人体内唯一可以作为葡萄糖传感器的HK。
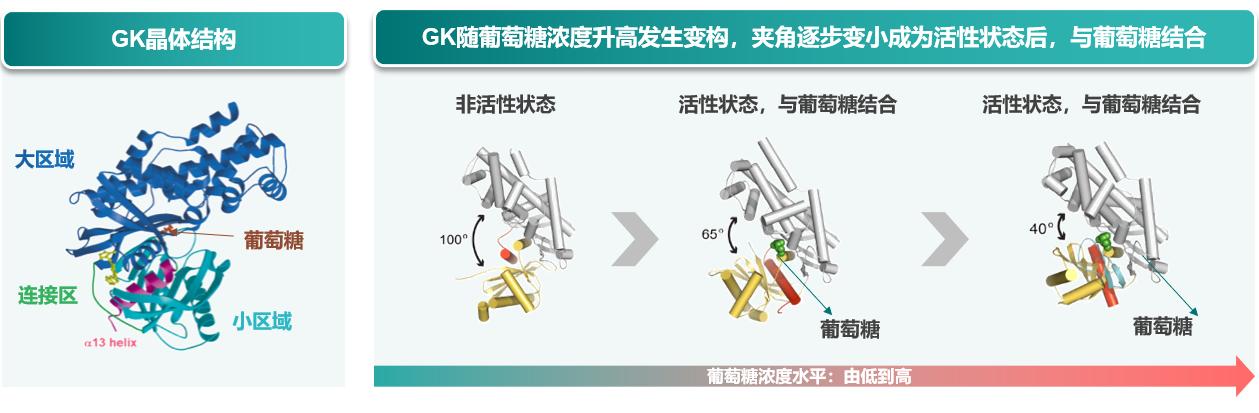
GK本身是单体变构酶,其分子结构类似于“夹子”,在人体内存在三种构象,会随着葡萄糖浓度变化而变化:当葡萄糖浓度较低时,GK不与葡萄糖结合,处于非活性状态;当体内葡萄糖浓度升高时,GK与葡萄糖结合,处于活性状态。
始于第一步,贯穿每一步
GK可调动血糖核心调控器官的适时启动,形成血糖稳态调控回路
GK同时存在各核心调糖靶器官(肝脏、胰腺及肠道),是血糖调控核心器官细胞内葡萄糖代谢第一个关键酶,当GK敏锐感知到葡萄糖浓度到达葡萄糖调定点后,将葡萄糖信号转换为各器官响应,开启后续的自主调糖机制。
在胰岛β细胞中,当人体在葡萄糖摄取之后,血糖浓度高于5 mmol/L,GK就会被激活,促进胰岛素的分泌;逐渐升高的胰岛素作用于肝脏细胞,促进肝细胞GK的基因表达,为其发挥作用提高足够量的GK。当血糖浓度升至10 mmol/L时,GK与葡萄糖调控蛋白解离,前者在肝细胞质中恢复酶的活性,启动肝糖原合成,通过GK的作用,机体最为重要的葡萄糖感知细胞和葡萄糖处置细胞相互协调,维持血糖稳态。
同时,在肠道内分泌细胞中,随着葡萄糖水平增加,GK激活启动胰高糖素样肽-1(GLP-1)分泌,GLP-1可进一步促进β细胞的GK活性和胰岛素分泌增加。
此外,还有研究发现,GK在下丘脑中发挥作用。1)葡萄糖兴奋神经元中的GK将葡萄糖磷酸化后,导致KATP通道关闭,神经元去极化触发Ca2+通道打开,进而分泌神经递质调节血糖稳态;而在葡萄糖抑制神经元中GK可诱导ATP水平增加,来刺激Na+/K+ ATP泵完成神经元超极化,从而抑制神经元活动。GK在垂体前叶细胞中也被证实存在葡萄糖传感功能,但具体机制有待进一步探索。2)在葡萄糖抑制神经元中GK可诱导ATP水平增加,来刺激Na+/K+ ATP泵完成神经元超极化,从而抑制神经元活动,大多数葡萄糖兴奋神经元表达厌食性肽,而葡萄糖抑制神经元在低血糖状态下释放刺激食欲的肽来增加摄食。进食引起的胃肠道机械感受器受刺激后产生的饱腹感信号,通过迷走神经传导至脑干,另外一方面,食物刺激肠道GLP-1和GIP的释放进一步影响胰岛素和胰高糖素的释放来维持血糖稳态。
作为血糖调控核心器官细胞内葡萄糖代谢第一个关键酶,GK可将各个核心器官的响应有机串联,是机体保持血糖稳态自主调节的核“芯”。
修复GK,重塑稳态自主调节为T2DM治疗带来新的希望
兼听则明,偏信则暗,血糖稳态自主调节亦如此。GK一旦功能受损,就会影响整个调节系统的敏锐度和缜密性,导致系统自主调节失常,机体对骤然升高的血糖“视而不见”,血糖稳态无法维持,导致糖代谢紊乱,血糖失稳态加剧靶器官功能损坏,陷入恶性循环。
GK功能降低导致的血糖失稳态恰恰是T2DM的发病关键。研究显示,2型糖尿病(type 2 diabetes mellitus,T2DM)患者普遍存在GK损伤,GK功能显著降低。Del Guerra 等采用T2DM和正常人胰岛离体细胞进行研究后,发现相比正常人群,T2DM患者胰岛细胞数量约减少10%,而GK基因表达约降低40%;葡萄糖刺激的胰岛素分泌量下降了大约50%,且早相胰岛素分泌高峰消失。另一项在对患肥胖型糖尿病的个体及正常肥胖个体的GK活性研究中,发现患有肥胖型糖尿病的个体肝脏GK活性较正常组下降近50%,可见GK的正常功能是稳态系统自主调节的关键。
葡萄糖激酶通过启动多细胞多器官的精密协作维持血糖稳态,在人体血糖稳态调控中发挥着核心作用,对于2 型糖尿病新型药物研发的有着重大的意义。半个世纪以来,科学家们持续致力于GK通路的药品研发。自从2001年公开葡萄糖激酶激活剂(GKA)的药理学基础以来,有关GKA的研发就成为改变T2DM治疗理念的全新希望!
